
(lat. atomus, gr. atomos, insécable)
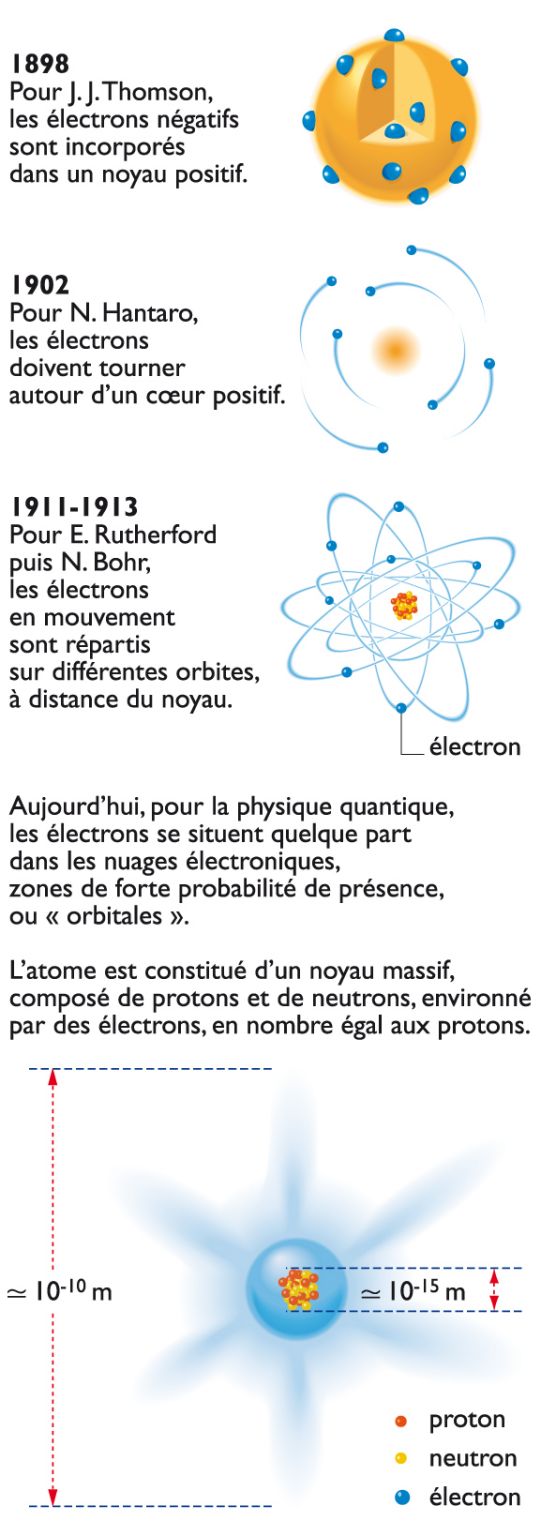
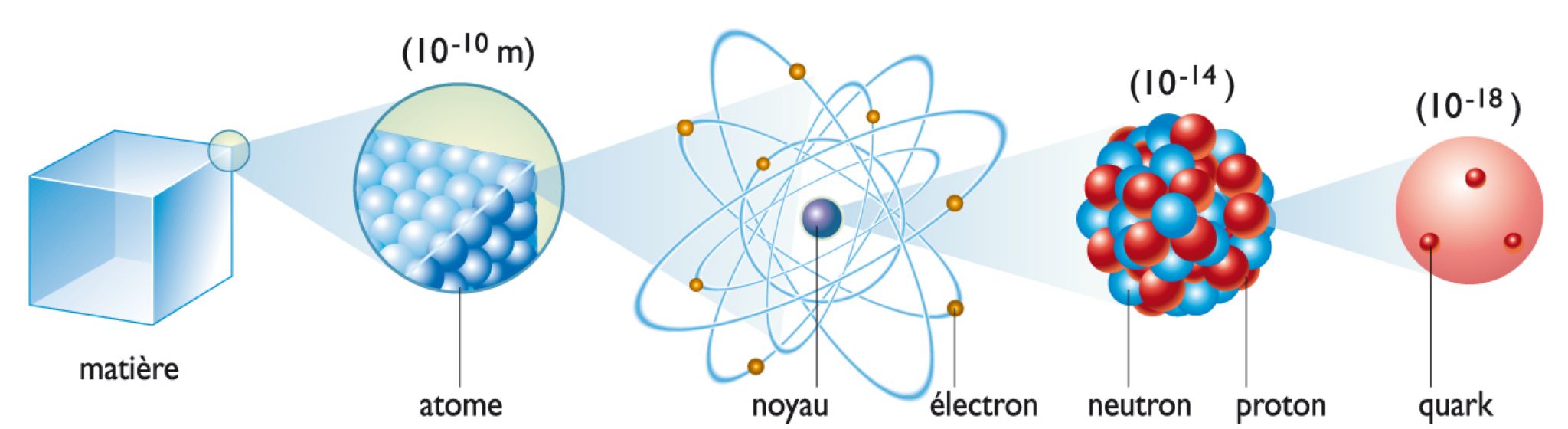


L'atome comporte un noyau central massif environné d'un nuage de particules de charge négative, les électrons. Le noyau est lui-même composé de deux types de particules : les neutrons, sans charge électrique, et les protons, chargés positivement. Dans un atome électriquement neutre, le nombre de protons est identique à celui des électrons. Ce nombre, différent pour chaque élément chimique, désigne le numéro atomique de chacun des 92 éléments existant dans la nature (90 éléments stables et 2 instables, le technétium [43] et le prométhéum [61]). Par exemple, l'atome d'hydrogène a le numéro 1, celui d'uranium le numéro 92, etc. Par ailleurs, il peut y avoir, pour un élément donné, des noyaux d'atome plus lourds ou plus légers, les isotopes, composés d'un plus grand ou d'un plus petit nombre de particules neutres (les neutrons). Ainsi, le carbone à 16 isotopes, dont le célèbre carbone 14.
Propriétés de l'atome.
Selon une conception due à N. Bohr, le nuage électronique qui entoure le noyau est réparti en couches, un niveau d'énergie correspondant à chaque couche. La couche externe, la plus éloignée du noyau, peut comporter plus ou moins d'électrons : ce sont eux dont les interactions avec les électrons d'autres atomes sont responsables des liaisons chimiques donnant les molécules des corps composés. Les atomes peuvent aussi gagner ou perdre un ou plusieurs électrons, formant alors des « ions » (anions chargés négativement, cations chargés positivement). Les propriétés chimiques des corps dépendent donc essentiellement du nombre d'électrons présents sur cette couche externe, dite couche de valence. Par exemple, le sodium et le potassium ont des propriétés chimiques analogues qui s'expliquent par la présence sur cette couche d'un électron unique.
Les noyaux des atomes les plus lourds sont radioactifs : ils se transforment, par désintégration, en un autre élément tout en émettant des rayonnements. Certains (uranium, plutonium) peuvent, sous l'action de neutrons, se fissionner en noyaux plus légers en éjectant des neutrons et en libérant une grande quantité d'énergie (réacteur nucléaire, bombe A). Les noyaux des atomes les plus légers peuvent, au contraire, fusionner en libérant aussi une intense énergie (étoiles, bombe H).