
adjectif
(lat. acidus)
PÉDOLOGIE Sol acide, dont le pH est inférieur à 6,5.
nom masculin
CHIMIE Corps hydrogéné dont la solution dans l'eau fournit des ions H3O+, qui agit sur les bases et les métaux en formant des sels, et qui fait virer au rouge la teinture bleue de tournesol.
Les acides sont caractérisés par un ensemble de propriétés que partagent un grand nombre d'espèces chimiques. À l'acidité correspond une saveur : le vinaigre pique la langue. Les acides minéraux ont une action sur la liqueur de tournesol, qu'ils colorent en rouge, sur d'autres solutions, appelées indicateurs colorés, comme l'hélianthine, qui devient rouge-orangé. Ils attaquent de nombreux métaux en formant des sels ; ils neutralisent les bases.
La fonction acide.
Elle se caractérise principalement par le fait que, dans une réaction chimique, un acide libère des ions positifs d'hydrogène (H+). Ces ions H+ sont les « hydrogènes acides ». Les composés, tel l'acide sulfhydrique (H2S), où l'hydrogène acide est uni à un non-métal autre que l'oxygène, sont appelés hydracides ; ceux qui, tel l'acide sulfurique (H2SO4), contiennent de l'oxygène sont des oxacides.
Avec du papier-pH ou un pH-mètre, on mesure le « degré » d'acidité que l'on associe à un nombre, le potentiel hydrogène ou pH, lié à la concentration d'hydrogènes acides. Tandis que l'eau pure ne contient qu'un ion H+ pour 550 millions de molécules, ce qui correspond à un pH neutre (égal à 7), l'addition de jus de citron ou de vinaigre apporte à celle-ci un supplément d'ions H+, ce qui a pour effet de diminuer le pH de la solution acide ainsi obtenue. Par ailleurs, on distingue les acides forts (acide chlorhydrique, acide nitrique), entièrement dissociés en ions dans l'eau, et les acides faibles (acide acétique, acide carbonique), qui ne le sont que partiellement.
Les acides et la vie.
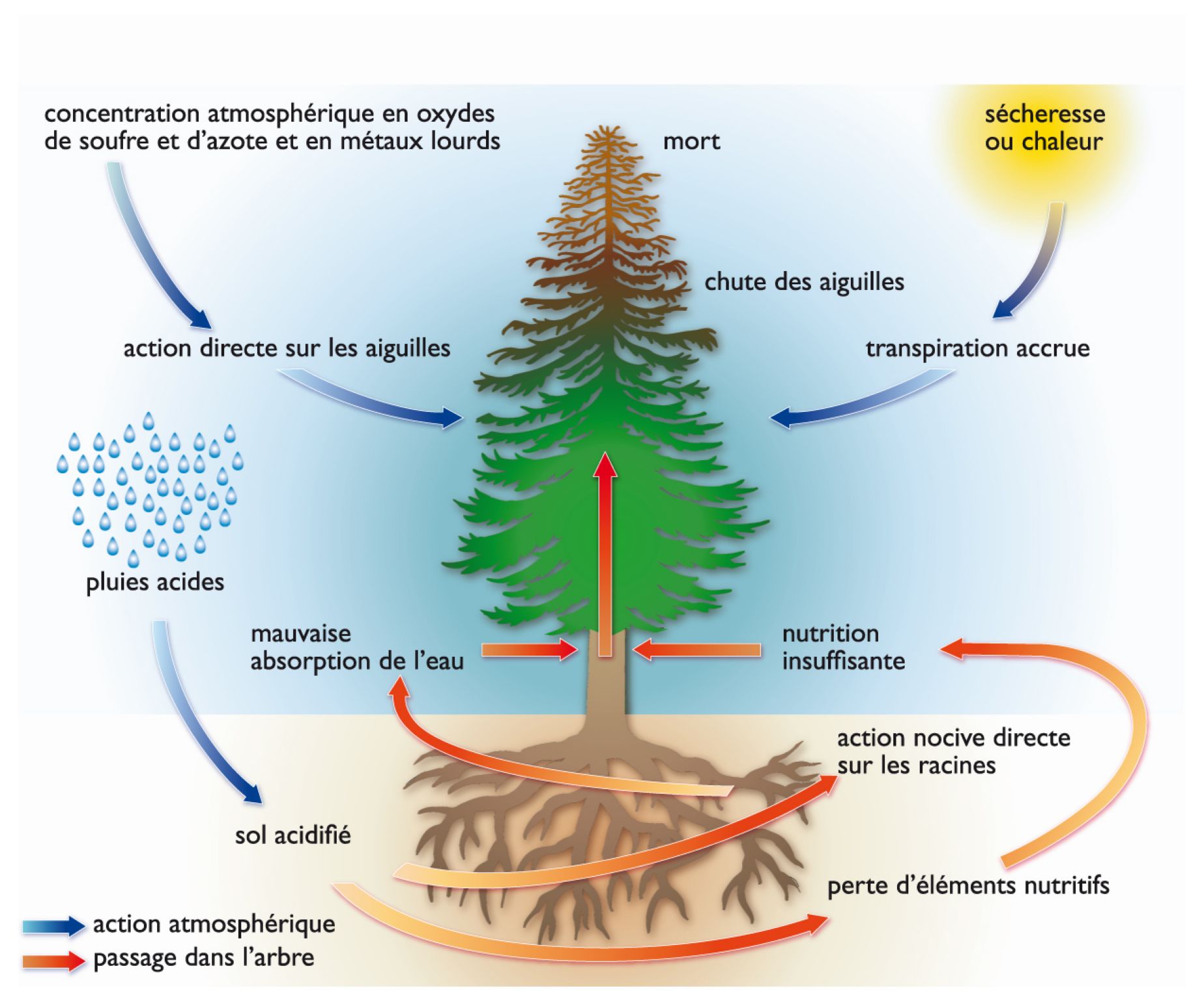
Dans la vie quotidienne, l'acidité est diversement présente. Le lait, les fruits et les légumes sont acides. Il existe des sols naturellement acides, par exemple les terres siliceuses ou marécageuses. En agriculture, la mesure du pH des sols est nécessaire pour déterminer la culture la plus adaptée. La pollution atmosphérique par les activités industrielles ou urbaines offre un exemple de l'effet des acides sur l'environnement. Les cheminées ou les pots d'échappement rejettent dans l'air des oxydes d'azote et de l'anhydride sulfureux qui ne sont autres que des acides déshydratés. Les vents entraînent parfois sur des milliers de kilomètres ces polluants, qui, au contact des micro-gouttelettes nuageuses ou des gouttes de pluie, se transforment pendant leur course en acide sulfurique et en acide nitrique, à l'origine des pluies acides.
Enfin, au niveau le plus élémentaire de la vie, celui de la cellule, les acides sont, au même titre que les bases, des constituants fondamentaux de la matière organique. Ainsi, toutes les protéines qui constituent la matière vivante sont formées d'une infinité de combinaisons de seulement 23 acides aminés (ou aminoacides), et seulement 21 chez l'homme. Par ailleurs, les macromolécules porteuses de l'information nécessaire au développement et au fonctionnement des organismes sont aussi des acides : acides nucléiques ADN et ARN.